Clariscience ha partecipato al 63° Simposio AFI
dal 5 al 7 giugno 2024



HAI VISITATO IL NOSTRO STAND?
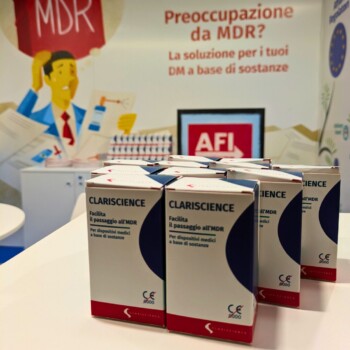
Se non sei riuscito a visitare il nostro stand, e sei curioso di scoprire cosa abbiamo realizzato per la nostra prima partecipazione al SIMPOSIO AFI, puoi dare uno sguardo qui sotto.
Clariscience ha presentato un servizio specifico per i fabbricanti di dispositivi medici a base di sostanze, consapevole delle criticità da affrontare per dimostrarne la conformità all’MDR.
COSA TI OFFRIAMO?
- Verifica della classificazione del dispositivo
- Approfondimenti sui meccanismi d’azione delle sostanze
- Ricerche di dati ADME
- Verifica della biocompatibilità del dispositivo
- Razionali giustificativi in caso di presenza di sostanze CMR
- Verifica e valutazione del livello di evidenza clinica
- Definizione della tipologia di raccolta dati clinici necessaria e sufficiente
- Affiancamento nelle relazioni con le CRO
- Ricerche bibliografiche sistematiche per sostanziare razionali giustificativi
COSA PREPAREREMO PER IL PROSSIMO ANNO?
Per ora non possiamo svelarti nulla, ma siamo già al lavoro per rendere la nostra partecipazione ancora più vicina alle necessità dei partecipanti. Nell’attesa guarda cosa abbiamo presentato quest’anno.
Speciale AFI
Per aiutarti nel percorso di sviluppo del tuo dispositivo medico e garantire la conformità ai requisiti del Regolamento, abbiamo creato una guida dedicata per offrire una panoramica chiara e accessibile dei punti salienti della MDCG 2022-5.
La linea guida MDCG 2022-5 “Guidance on borderline between medical devices and medicinal products under Regulation (EU) 2017/745 on medical devices” fornisce indicazioni cruciali per identificare correttamente i prodotti che possono essere classificati sia come dispositivi medici che come medicinali, aiutando i fabbricanti a seguire il percorso regolatorio appropriato.
In questo modo potrai avere un’eccellente base di partenza per esplorare i concetti chiave nell’analisi dei casi dubbi in cui un prodotto sembrerebbe poter essere classificato sia come dispositivo medico che medicinale.
Scarica la guida
Compila il form e ricevi il link per scaricare la guida per la lettura della MDCG 2022-5.
COSA PUò FARE CLARISCIENCE PER TE?
IL MONDO DEI DISPOSITIVI MEDICI TI INCURIOSISCE?
Ogni settimana pubblichiamo interessanti approfondimenti sul settore dei dispositivi medici e IVD, e sull’intero mondo life science.
Leggi il nostro blog, resta informato e non perderti gli ultimi aggiornamenti.