SCOPRI DI PIÙ
SCOPRI DI PIÙ
 SCOPRI DI PIÙ
SCOPRI DI PIÙ
 SCOPRI DI PIÙ
SCOPRI DI PIÙ

Affari regolatori
Per dispositivi medici e IVD

Sistemi di gestione
per la qualità
Per dispositivi medici e IVD

Medical writing e comunicazione scientifica
Per il mondo life science
Non sai quale fra i nostri servizi fa per te?
Seleziona l’area di tuo interesse e orientati usando la nostra guida.
Clariscience annuncia la sua partecipazione al prestigioso 63° Simposio AFI che si terrà a Rimini dal 5 al 7 giugno…
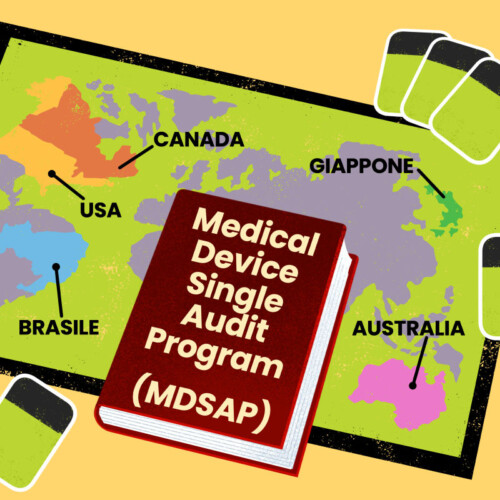
MDSAP è un programma di audit che consente la valutazione della conformità del Sistema di Gestione per la Qualità (SGQ)…
La revisione regolatoria di un protocollo o di un report di uno studio clinico è un passaggio cruciale nel processo…
Un dispositivo medico adattabile è un dispositivo medico prodotto in serie, che per conseguire la propria destinazione d’uso deve essere…
Il Riesame da parte della Direzione è il momento in cui l’organizzazione tira le somme del periodo in esame (di…
Come possiamo capire la rilevanza della rivista focalizzandoci solo sull’area di interesse? Esiste un modo, ed è quello della consultazione…
I requisiti relativi all’etichettatura dei dispositivi medici disposti dall’ U.S. FDA sono elencati all’interno del Codice dei Regolamenti Federali (CFR).
L’MDR ha introdotto varie novità, tra le quali sicuramente l’attribuzione di compiti specifici in capo, non più solo ai fabbricanti…
Esistono numerose risorse a supporto dei medical writer per migliorare le competenze statistiche e affrontare le sfide nell’analisi dei dati.
L’articolo 22 dell’MDR, che disciplina la fabbricazione, la sterilizzazione e la commercializzazione di sistemi e kit procedurali, rappresenta un pilastro…
La serenità dell’ambiente di lavoro, lungi dall’essere obbligo o imposizione di dover essere così, è invece una volontà forte e…
La selezione delle risorse umane risulta essere un processo estremamente importante e particolarmente critico, a cui le organizzazioni che operano…
Siamo informatori scientifici alla nostra millesima visita dal medico e, dopo esserci informati sullo stato di salute di tutte le…
Secondo quanto indicato all’articolo 110 del IVDR sulle disposizioni transitorie, la condizione essenziale da rispettare per immettere sul mercato o…
In seguito all’entrata in vigore del MDR anche importatori e distributori devono rispettare obblighi specifici e cooperare con i fabbricanti…
La redazione del protocollo è un passaggio fondamentale nella fase di pianificazione di una ricerca clinica. Questo documento integra informazioni…
I corsi di formazione di Clariscience
Le tematiche principali e più attuali relative agli affari regolatori e alla qualità di dispositivi medici e IVD, e al medical writing e alla comunicazione scientifica per l'intero mondo life science.
Speed webinar
Comunicazione scientifica
23 Maggio 2024
ore 16:00
1 h
Gratuito
Zoom
Come costruire opportunamente una bibliografia per uno studio clinico in ambito scientifico.
4 Giugno 2024
ore 16:00
1 h
Gratuito
Zoom
Webinar dedicato alle novità più rilevanti che il Regolamento Dispositivi Medici ha introdotto per tutti i dispositivi a base di sostanze.
25 Giugno 2024
ore 10:30
2 h
350€
Zoom
Contenuti dello Speed Webinar Nonostante le statistiche descrittive siano il punto di inizio di qualunque analisi di dati, non sempre alcune grandezze chiave – per prime media, moda e mediana...
In collaborazione con Prof. Davide Radice
16 Luglio 2024
ore 16:00
1 h
Gratuito
Zoom
Il webinar affronterà i diversi step del processo di progettazione di un dispositivo medico.
Prova Raqa Underground!
RAQA Underground è la mappa interattiva che racconta in modo visuale affari regolatori e quality assurance del mondo dei dispostivi medici.