Tutti gli articoli scritti da Annarita Berlese
Annarita Berlese
Regulatory Affairs Executive
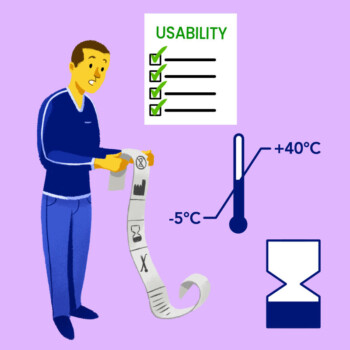
L’etichettatura è un elemento fondamentale per garantire l’uso sicuro ed efficace di un dispositivo medico da parte degli operatori professionali…
Il “Point of Care” è inteso in senso più ampio come “luogo vicino al paziente” o come luogo all’interno della…
Scopriamo assieme come avviene lo scambio commerciale dei dispositivi medici tra Unione Europea e Svizzera e qual è la regolamentazione…
L’FDA pone attenzione all’interazione tra utilizzatore e dispositivo medico. Per poter commercializzare un dispositivo medico negli Stati Uniti è necessario…
Un dispositivo medico adattabile è un dispositivo medico prodotto in serie, che per conseguire la propria destinazione d’uso deve essere…
Secondo quanto indicato all’articolo 110 del IVDR sulle disposizioni transitorie, la condizione essenziale da rispettare per immettere sul mercato o…
Quali sono i requisiti per l’immissione in commercio dei dispositivi medici su misura (custom made)? Le tecnologie di produzione non…
Il processo di dimostrazione della conformità ai nuovi requisiti normativi, considerando che è necessario coinvolgere anche un organismo notificato, può…